La pandémie de Covid-19 a accéléré le recours à des interactions à distance entre investigateurs d’essais cliniques et patients et l’adoption de nouvelles technologies numériques. Cela a favorisé la décentralisation du SCAC, avec tous les avantages qui en découlent. Explications avec MultiHealth.
Le SCAC, Suivi Clinique Après Commercialisation (en anglais PMCF, Post Market Clinical Follow-up), est un processus continu de mise à jour de l’évaluation clinique. Le fabricant collecte des données cliniques résultant de l’utilisation d’un dispositif médical (DM) en vie réelle, et les évalue de manière proactive pour confirmer les revendications de performances et de sécurité, pendant toute la durée de vie prévue du DM.
La décentralisation offre la possibilité, grâce à des outils numériques, de repenser l’investigation clinique en la rapprochant au plus près de la source de données, à savoir le patient. La distance sociale imposée par le confinement a renforcé cette tendance de manière significative.
Le rôle central des outils digitaux
La décentralisation implique la dématérialisation, c’est-à-dire le recours à des technologies numériques, à la fois par les fabricants, les professionnels de santé et les patients.
La téléconsultation a été d’un grand secours pendant la crise du Covid-19, son déploiement ayant pris de l’ampleur en raison des conditions sanitaires. Cette modalité de consultation est maintenant entrée dans les habitudes des professionnels de santé et des patients. Ces entretiens par vidéo permettent non seulement de maintenir un contact de proximité avec le patient, mais également d’évaluer à distance si les patients utilisent correctement un appareil, ce qui présente un intérêt supplémentaire dans le cadre d’investigations cliniques spécifiques à un DM.
Le nombre de dispositifs médicaux connectés s’est démultiplié ces dernières années. Intégrés à des plateformes de télésurveillance, ils permettent la remontée en temps réel de données patient telles que la fréquence cardiaque, la qualité de sommeil ou le degré d’activité physique. A côté de ces DM, il existe des objets connectés de santé comme les balances ou tensiomètres connectés. Lorsque ces objets ont fait la preuve de leur fiabilité, ils peuvent être inclus dans le suivi clinique post-commercialisation de dispositifs médicaux, y compris en vue de collecter des données liées à la prévention, la réduction de risque ou l’impact sur l’évolution de
pathologies chroniques.
La dématérialisation implique la digitalisation des formulaires utilisés dans les investigations cliniques, une pratique déjà largement répandue,
qu’il s’agisse de :
- recueillir le consentement patient (e-consent),
- collecter des informations saisies directement par le patient (e-PRO, Patient Report Outcome)
- ou réunir des informations recueillies par l’équipe médicale (e-CRF, Case Report Form) incluant des données démographiques, cliniques, …
Enfin, une composante essentielle de la décentralisation des investigations cliniques est le monitoring des données source à distance (rSDV, remote Source Data Verification). En règle générale, le monitoring garantit la fiabilité des données recueillies et renforce donc la qualité de l’étude. En France, en avril 2021, la CNIL a publié des recommandations provisoires concernant la réalisation du contrôle qualité à distance des données sources.
Depuis le 31 décembre 2021, ces recommandations ne sont plus en vigueur. A ce jour, il n’existe aucun référentiel, aucune Méthodologie de Référence (MR) adaptée aux essais cliniques digitalisés, laissant penser qu’il n’est plus possible d’avoir recours à cette modalité de monitoring à distance. Pourtant, le rSDV est toujours et plus que jamais d’actualité : il se pratique via une plateforme sécurisée, validée, dédiée à cet effet, et autorisée par la CNIL pour chaque étude. L’absence de MR signifie qu’un process de soumission spécifique CNIL est à anticiper, au même titre que la soumission CNRIPH.
Impliquer les fournisseurs locaux de soins de santé
Les professionnels paramédicaux contribuent en local aux soins et à l’amélioration des conditions et de la qualité de vie des patients. Trop peu intégrés ce jour dans la conception d’investigations cliniques, ils jouent pourtant un rôle clé dans le parcours patient. Ces professionnels incluent :
- les soignants : infirmiers, aide-soignants, sagesfemmes,
puériculteurs… - les professionnels de la rééducation : psychomotriciens, masseurs-kinésithérapeutes, diététiciens, nutritionnistes…
- les métiers de l’appareillage : opticiens-lunetiers, orthoptistes, audioprothésistes, orthophonistes,pédicures, podo-orthésistes…
Former ces équipes investigatrices mobiles aux Bonnes Pratiques Cliniques (ISO 14155) et au contexte réglementaire des DM permettrait de déployer des SCAC efficients. En effet, bien qu’aujourd’hui peu sollicités, ces métiers représentent un levier important pour recueillir des données de qualité et maintenir l’engagement dans la durée des patients participant à des suivis cliniques parfois longs.
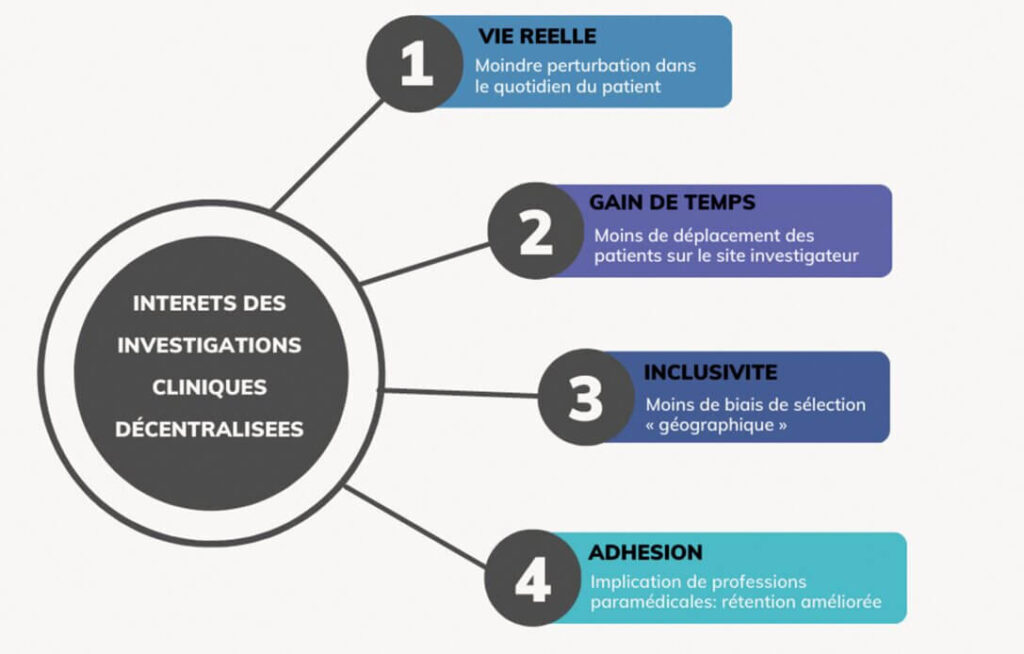
Les bénéfices de la décentralisation
La décentralisation est rarement envisagée en mode 100%. Les études menées avec le support de technologies numériques et outils digitaux sont en effet le plus souvent hybrides avec des visites limitées sur site investigateur associées à une communication à distance avec le patient. Dans ce contexte, les bénéfices sont multiples, comme le montre la figure ci-dessus.
- Reflet de la vie réelle : l’adoption de méthodes décentralisées contribue à recueillir des données hors environnement clinique, avec une perturbation
moindre du quotidien du patient et sans intervention sur les modalités usuelles d’utilisation. Ces méthodes de recueil plus « discrètes » reflètent davantage les situations réelles post-commercialisation. - Gain de temps : collecter de la donnée via des investigations cliniques décentralisées permet de réduire la durée des investigations, le déplacement des patients sur le site investigateur n’étant plus une condition sine qua non au recueil d’informations.
- Inclusivité : les autorités de santé et organismes notifiés exigent une représentativité la plus exhaustive possible des patients « bénéficiaires ». En déployant les investigations au plus près des patients, notamment grâce aux technologies numériques, le biais de sélection « géographique » est limité et la diversité des patients participants accrue.
- Adhésion : la mobilisation de professions paramédicales proches du quotidien des patients permet de renforcer l’adhésion des patients à l’étude et de garantir le recueil d’un volume de données plus important dans le temps. Cette rétention améliorée est également un gage de représentativité.
La décentralisation des investigations cliniques permet de désenclaver les SCAC en réduisant la dépendance à l’égard des infrastructures traditionnelles de recherche spécialisées dans la collecte de données. Il existe cependant des DM ou DM-DIV (dispositifs médicaux de diagnostic in vitro) dont l’utilisation en pratique dépend uniquement d’un expert clinique hautement qualifié ou formé. Par exemple, les suivis au long cours de dispositifs liés au diagnostic ou à certaines procédures, comme l’utilisation de scanners ou de cathéters, ne sont pas éligibles à la décentralisation.
En conclusion, la méthodologie des essais cliniques décentralisés accélérée par la pandémie de Covid-19 représente aujourd’hui un changement fondamental dans la façon dont les évaluations cliniques sont menées. Ces modifications de pratique bénéficient au suivi clinique après commercialisation des dispositifs médicaux. Cela demande de former les parties prenantes – dont les professions paramédicales – aux investigations cliniques et d’adapter les modèles de service pour faciliter l’utilisation des solutions digitales et leur validation par les instances réglementaires.
La décentralisation permet de collecter des données de vraie vie auprès d’une population de patients plus représentative. Une agilité au service de la diversité.
Questions fréquentes
Besoin d’accompagnement ?
Vous planifiez un SCAC ou une investigation clinique décentralisée ? CLINACT, entité du Groupe MultiHealth, vous accompagne dans la conception, le monitoring à distance (rSDV) et la soumission réglementaire (CNRIPH, CNIL) de vos études post-commercialisation.



